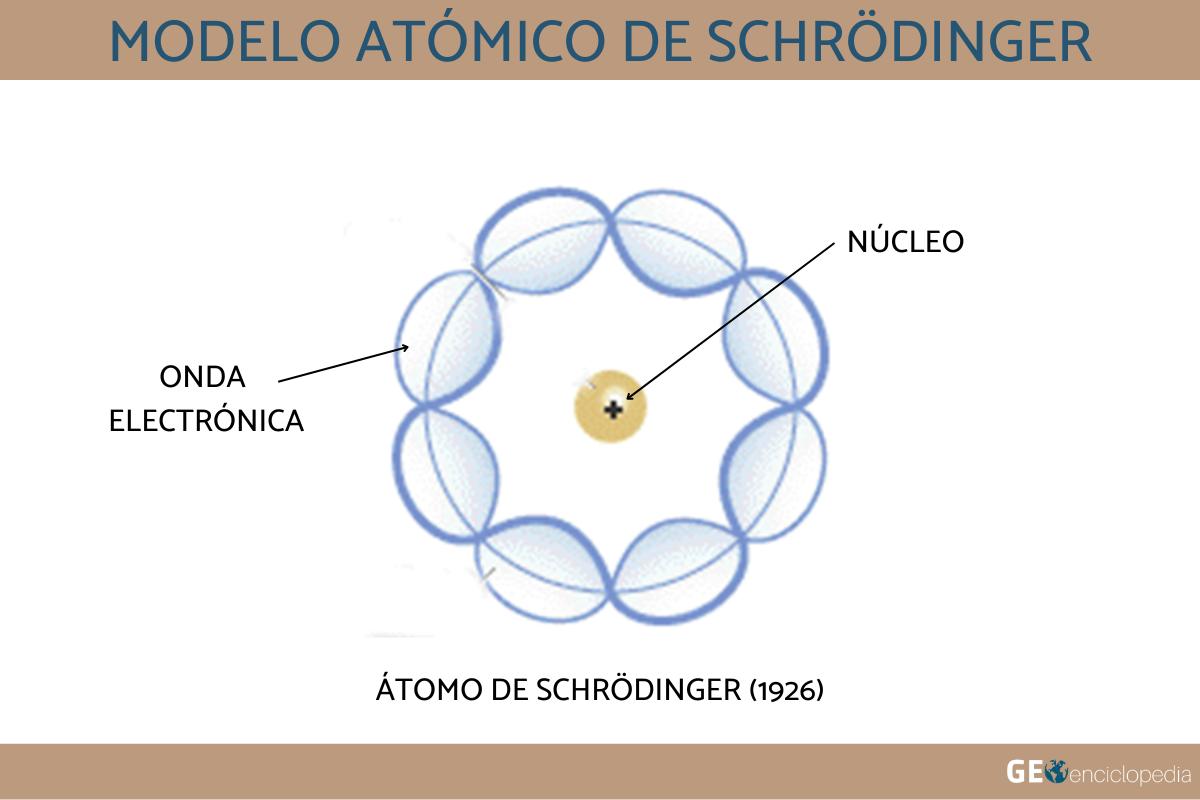
El Modelo Atómico de Schrödinger: El Fundamento de la Mecánica Cuántica
El Modelo Atómico de Schrödinger es una de las bases fundamentales de la mecánica cuántica, la teoría física que describe el comportamiento de las partículas subatómicas. Desarrollado por el físico austriaco Erwin Schrödinger en la década de 1920, este modelo revolucionó nuestra comprensión de la estructura atómica y abrió las puertas a un nuevo mundo de posibilidades en la física.
Antecedentes y Contexto Histórico
Antes de la formulación del modelo de Schrödinger, la teoría atómica estaba basada en el modelo de Bohr, que describía a los electrones orbitando alrededor del núcleo en órbitas definidas. Sin embargo, este modelo presentaba algunas limitaciones, como la incapacidad de explicar la estabilidad de los átomos con más de un electrón.
En este contexto, Erwin Schrödinger propuso un enfoque diferente, basado en las ecuaciones de onda. Inspirado en trabajos anteriores de Louis de Broglie y Max Planck, Schrödinger desarrolló una ecuación que describe el comportamiento de una partícula subatómica en términos de una función de onda compleja.
La Ecuación de Schrödinger
La ecuación de Schrödinger es la piedra angular del modelo atómico del mismo nombre. Esta ecuación describe cómo evoluciona la función de onda de una partícula en el tiempo y en el espacio. La función de onda contiene toda la información necesaria para determinar la probabilidad de encontrar la partícula en una posición y momento dados.
La ecuación de Schrödinger es una ecuación diferencial parcial que tiene la forma:
\[i\hbar \frac{\partial}{\partial t} \Psi(\mathbf{r},t) = \hat{H}\Psi(\mathbf{r},t) \]
Donde:
– \(i\) es la unidad imaginaria,
– \(\hbar\) es la constante reducida de Planck,
– \(\Psi(\mathbf{r},t)\) es la función de onda,
– \(\mathbf{r}\) es el vector de posición,
– \(t\) es el tiempo, y
– \(\hat{H}\) es el operador hamiltoniano, que representa la energía total del sistema.
Interpretación Probabilística
Una de las características más distintivas del modelo de Schrödinger es su interpretación probabilística. Según la mecánica cuántica, la posición y el momento de una partícula no pueden conocerse con certeza, sino que se describen a través de distribuciones de probabilidad dadas por la función de onda.
La interpretación probabilística de la mecánica cuántica ha sido objeto de numerosos debates y discusiones filosóficas a lo largo de los años. Algunos físicos argumentan que esta interpretación refleja la verdadera naturaleza del mundo cuántico, mientras que otros la consideran una limitación de nuestro conocimiento y capacidad de medición.
Orbitales Atómicos y Números Cuánticos
En el modelo de Schrödinger, los electrones en un átomo se describen a través de funciones de onda tridimensionales llamadas orbitales atómicos. Estos orbitales representan las regiones donde es más probable encontrar a los electrones, y se caracterizan por números cuánticos que determinan sus propiedades.
Existen cuatro números cuánticos principales que se utilizan para describir los orbitales atómicos:
– Número cuántico principal (\(n\)): Determina la energía y tamaño del orbital.
– Número cuántico azimutal (\(l\)): Determina la forma del orbital.
– Número cuántico magnético (\(m_l\)): Determina la orientación espacial del orbital.
– Número cuántico de espín (\(m_s\)): Describe la orientación del espín del electrón.
Estos números cuánticos son fundamentales para comprender la estructura electrónica de los átomos y predecir su comportamiento químico.
Forma y Orientación de los Orbitales
Los orbitales atómicos tienen formas características que dependen del número cuántico azimutal (\(l\)). Por ejemplo, los orbitales \(s\) tienen forma esférica y son los más simples, mientras que los orbitales \(p\) tienen forma de lóbulos y presentan una orientación específica en el espacio.
La combinación de estos orbitales permite formar enlaces químicos y determinar la geometría de las moléculas. La teoría de los orbitales moleculares, basada en el modelo de Schrödinger, es fundamental en química computacional y en el diseño de nuevos compuestos químicos.
Aplicaciones Prácticas y Tecnológicas
El Modelo Atómico de Schrödinger tiene numerosas aplicaciones en la física y la química modernas. Desde la predicción de propiedades de materiales hasta el diseño de fármacos, la mecánica cuántica basada en el modelo de Schrödinger ha revolucionado muchos campos de la ciencia.
Química Computacional
En química computacional, se utilizan métodos basados en la mecánica cuántica para simular la estructura y propiedades de moléculas y materiales a nivel atómico. Estos cálculos son fundamentales para la investigación en química y para el diseño de nuevos compuestos con aplicaciones en medicina, electrónica y energía.
Física de Materiales
En la física de materiales, el modelo de Schrödinger es esencial para entender las propiedades de los sólidos y predecir su comportamiento en diferentes condiciones. La teoría de bandas, que describe la estructura electrónica de los materiales cristalinos, se basa en la mecánica cuántica y en el modelo de Schrödinger.
Desafíos y Futuro de la Mecánica Cuántica
A pesar de sus logros y aplicaciones, la mecánica cuántica basada en el modelo de Schrödinger todavía enfrenta desafíos y preguntas sin responder. La interpretación de la función de onda, la naturaleza de la superposición cuántica y la relación entre la mecánica cuántica y la teoría de la relatividad siguen siendo temas de debate en la comunidad científica.
El futuro de la física cuántica promete emocionantes avances en campos como la computación cuántica, la teleportación cuántica y la criptografía cuántica. Estas tecnologías revolucionarias podrían cambiar por completo nuestra manera de entender y utilizar la información, abriendo la puerta a un mundo de posibilidades antes inimaginables.
En resumen, el Modelo Atómico de Schrödinger es una de las piezas fundamentales de la mecánica cuántica, una teoría que ha transformado nuestra visión del universo a nivel fundamental. Con sus aplicaciones prácticas y su potencial revolucionario, la mecánica cuántica basada en el modelo de Schrödinger sigue siendo un campo vibrante de investigación y descubrimiento en la ciencia moderna.